В то время, когда наши олигархи в 90-е растаскивали страну по карманам, наука в других странах активно развивалась. Были созданы не только инструменты и методы, но и новые дисциплины. Например, работы с геномом вируса, бактерии и клетки организма сегодня превратились в синтетическую биологию. Насколько такие работы продвинулись? До какого состояния дошло наше отставание на этом фронте? Может все-таки не навсегда? Ведь смогли наши ученые создать вакцину от эболы.
Далее подробнее об исследованиях, результаты которых поражают.
От вакцины против гриппа до методов, годящихся для экспедиции на Марс, ученые инженерно-биологических систем участвуют для удовлетворения медицинских потребностей 21-го века.
В марте 2013 года Китай объявил о том, что два человека умерли от инфекции птичьего гриппа. Этого конкретного штамма гриппа, известного как h7n9, ранее не было замечено у людей или животных, и не было вакцины. В последствии, когда вспышка распространилась, стало умирать больше людей. Ученые столкнулся с аналогичной ситуацией четырьмя годами ранее, когда появились пандемия гриппа H1N1. Несмотря на рекордный ответ для фармацевтической промышленности, созданию вакцины против H1N1 шло слишком долго, чтобы оказать реальное воздействие. На этот раз, против h7n9, ученые действовали заметно быстрее.
Этого конкретного штамма гриппа, известного как h7n9, ранее не было замечено у людей или животных, и не было вакцины. В последствии, когда вспышка распространилась, стало умирать больше людей. Ученые столкнулся с аналогичной ситуацией четырьмя годами ранее, когда появились пандемия гриппа H1N1. Несмотря на рекордный ответ для фармацевтической промышленности, созданию вакцины против H1N1 шло слишком долго, чтобы оказать реальное воздействие. На этот раз, против h7n9, ученые действовали заметно быстрее.
– Мы включились в работу, – говорит Сэмми Фара, президент синтетического подразделениея вакцин Геномики, Калифорния, чья компания уже готовится к этому сценарию с начала 2009.
В течение пяти дней, синтетическая Геномика, в партнерстве с Novartis, создала семенной вирус необходимый, чтобы начать производство вакцины. Обычно такая работа занимает от четырех до шести недель или даже дольше, - говорит Фара. Вакцина вскоре перешла на этап клинических испытаний и была закуплана правительством США в декабре 2013 года. Именно эта вакцина будет использоваться во время борьбы с второй волной инфекции h7n9, если это когда-нибудь случится.
С помощью средств синтетической биологии, компания обогнала старый метод производства вакцин. Это стало возможным благодаря дальновидному шагу со стороны Китая. Когда китайские органы здравоохранения объявили, что новый смертельный штамм гриппа был обнаружен, они одновременно опубликовали последовательности ДНК вируса. Это позволило Синтетической Геномике скачать важную информацию по гемагглютинину (H) и нейраминидазе (N) гена вируса, синтезировать их в лаборатории и объединить их с генным ‘костяком’ необходимым для вирусного роста и размножения. Затем вирус был быстро выращен в клетке производственной системы, составляющей основу вакцины, разработанной компанией «Новартис». Используя старые методы, физические образцы вируса должны были бы быть изолированы и создан вирус ослабленной версии, а затем выращен перед отправкой производителям для производства вакцин. Такой подход занял бы около пяти до шести месяцев.
– Хотя вспышка h7n9 не достигла масштабов пандемии, – говорит Фара, – синтетическая Геномика и Novartis использовали вспышку, чтобы продемонстрировать, что теперь они могут оперативно реагировать на подобные вызовы.
– После того, как последовательность генов с h7n9 стала доступна, мы смогли синтезировать эти гены в течение нескольких часов, – говорит Болин Хабби, глава исследования и разработки синтетических вакцин Геномики, добавив, что это был “простой и элегантный метод из арсенала синтетической биологии”.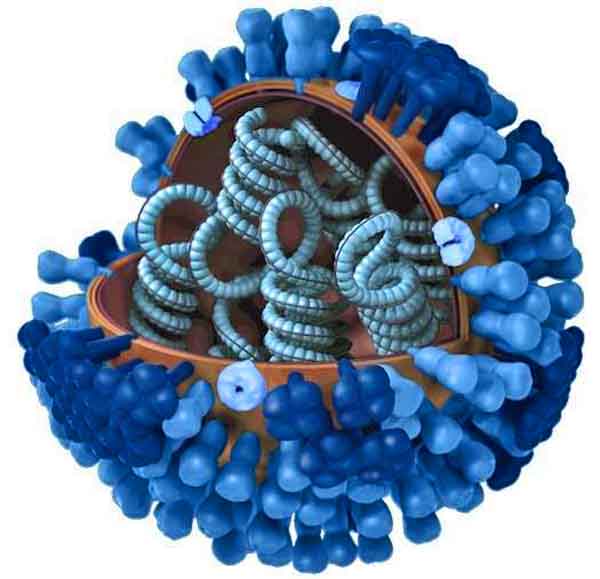
Синтетическая биология применяется также и по–другому. Например, в космическом путешествии на Марс, чтобы препараты могут быть изготовлены по требованию. Исследователи обращаются к синтетической биологии для решения сложных проблем 21 века. Эта технология стала возможной благодаря двум достижениям: недавняя способность синтезировать огромное количество ДНК чрезвычайно быстро, и наличием огромной вычислительной мощности.
Операционная система жизни
Как точно определить, что такое «синтетическая биология», Фара и Хабби заколебались дать быстрый ответ.
– Это хороший вопрос, – говорит Фара, посмеиваясь. Немного подумав, он добавляет:
–мы думаем о нем, как о модульном конструировании геномов, создавая клетки с определенными функциями. Синтетические биологи иногда сравнивают такой метод с программированием.
– Часто мы используем аналогию с операционной системой. Можно назвать ДНК и клетки как «операционная система жизни», - говорит Фара.
Синтетическая биология – это, в некотором роде, сложная версия генной инженерии, которая в своей основной форме была начата лишь десятилетия назад. Но есть и различия. Старомодный генно–инженерный метод добавляет или удаляет отдельные гены, которые как бы скачивают (или удаляют) новое программное обеспечение или приложения на ваш компьютер. Напротив, синтетическая биология переписывает всю вашу операционную систему и добавляет некоторые новые код одновременно.
– Это вопрос масштаба, - говорит Фарах. – В синтетической биологии разработаны совершенно новый метаболизм, гены и даже организмы с использованием принципов современной инженерии. Последовательности ДНК пишется как код, синтезированный в лаборатории и вставляются в клетку. Традиционные генно-инженерные методы не могут справиться с большими генными конструкции или целым геномом, – говорит Фара.
Традиционные генно-инженерные методы не могут справиться с большими генными конструкции или целым геномом, – говорит Фара.
Одним из пионеров синтетической биологии был Дж. Крейг Вентер, основатель синтетической Геномики. В 1995 году Вентер возглавлял команду, которая секвентировала первый клеточный геном бактерии Гемофильной инфекции[1]. А в 2001 году он возглавил собственный проект исследования последовательности генома человека[2], который шел вместе с проектом «геном человека». Он создал его в 2006 году, а в 2010 году объявил, что ему удалось создать синтетическую клетку, построенную из химически синтезированного генома и способную к репликации[3]. Фара характеризует его так:
– Крейг был в состоянии перейти от чтения генома к его написанию.
Совершенствовалась наука и технология, лежащая в ее основе. Вирусный геном, содержащий около 60 тысяч элементов, теперь может быть синтезированы за день; это было просто не возможно несколько лет назад.
– Более сложные геномы бактерий, содержащие миллионы элементов ранее, по старым технологиям заняла бы годы. Однако, теперь мы можем сделать это в течение нескольких недель или месяцев, – говорит Фара.
Причем эта работа включает в себя фазы проектирования, построения и тестирования, которое так важно для синтетической биологии.
– Это будет иметь большие последствия на дальнейшее развитие этой области науки. –добавляет он.
Синтетическая Геномика теперь может создавать вакцины практически для любого штамма гриппа в течение нескольких дней.
Лекарства по требованию
Один из самых больших успехов в синтетической биологии создание противомалярийного препарата «артемизинина». Этот препарат вырабатывается из китайский сладкий полыни, полыни однолетней, но только в крошечных количествах. Сконструированный штамм дрожжей теперь может производить препарат по запросу[4] и это
– гораздо лучше, чем завод. – говорит Джек Ньюмен, основатель микробной инженерной компании, Амирис.
Амирис, совместно с университетом Калифорнии, разработали технологию и запатентовали метод синтетической платформы в биологии. Но фармацевтическая компания Санофи обладает лицензией на производство артемизинина для поставки в развивающиеся страны на некоммерческой основе. Однако старая технология, производства артемизинина был медленной, потому что она занимала около года, ведь требовалось вырастить урожай сладкой полыни.
– Если бы вы были аграрием в Африке, вы затратили бы 18 месяцев, на выращивание препарата после оформления заказа, – говорит Ньюман. – У аграриев случались перебои, приводящие недопроизводству, - объясняет он. – Сейчас у нас есть стабильный способ, способный производить необходимое количество лекарства в течение месяца. Это также намного дешевле.
На фоне этого развиваются дрожжевая платформа, не прямолинейная, так называемый «полусинтетический артемизинин». Этот метод зародился в университете Калифорнии, в Беркли, в лаборатории Джэй Кеслинг. Последний имеет долгую и выдающуюся историю в области синтетической биологии. Чтобы двигать технологию вперед, Амириса, основанная в 2003 году четырьмя докторами в Беркли. Говорит Кеслинг
– Мы поняли, что происходящие в биологии новаторства, способны продвинуть фармацевтические разработки, – говорит Ньюман, один из докторов, – В то время мы называли это метаболический «ящик для гнструментов», но это не настолько круто, как синтетическая биология.
Ньюман говорит, что он и его коллеги собираются после работы, едят китайскую еду и предлагают свои идеи об областях применения этой новой науки для общего блага.
– Мы увидели, что производство артемизинина может иметь огромное значение, но не было особого финансового интереса, потому что малярия – проблема развивающегося мира.
Но в 2005 году они получили финансирование от Фонда Билла и Мелинды Гейтс.
В то время никто и никогда не проектировал организмы для производства абсолютно новых лекарств из-за сложности процесса. Ньюман считает, что шансы его были 1000 к 1. Первым делом нужно было найти гены в сладкой полыни, которые кодируют ферменты, необходимые для синтеза артемизинина, но ни один из этих генов не был выявлен.
– Университет в Беркли, имеет армию студентов, кандидатов и докторантов наук, работающих в этой области, – говорит он.
После полутора лет, они узнали все гены, необходимые для производства артемизинина из дрожжей. Но это было только тогда, когда Патрик Ковелло, ныне старший научный сотрудник Национального Институт биотехнологии растений научно–исследовательского Совета Канады, выявил более двух генов для производства. Производительность была несущественной.
На оптимизацию системы ушло два года. В этот момент Амириса совместно с Санофи наращивали производство. Теперь Амириса обладает большинством современных синтетических платформ биологии, направленные на производство лекарственных средств, известных как МюФарм(µPharm) и использует его, чтобы сделать продуктами, включая экологически чистое биотопливо и кожу, а также увлажняющий крем сквален. Команда Стэнфордского университета получила генетически модифицированные дрожжи для производства опиоидных препаратов тебаин и гидрокодон, которые ранее могли быть получены только из мака[5]
– Реинжиниринг дрожжей для производства различных химических соединений чем-то напоминает создание новых приложений для iPhone, – говорит Ньюман. – Так что, можно сказать, что когда я хочу создать молекулу, которая выглядит определенным образом, я уже знаю какие гены следует использовать для этого.
Ньюман описывает ферменты, как крошечные машины, которые точно присоседят углерода к углероду. Напротив, он говорит, что химический синтез молекул, сопоставим “замешиванием в кучу дерева и гвоздей вместе с помешиванием до состояния, когда получится дом”.
Технологии будущего
В синтетической биологии, ничего не оставлено на волю случая.
– Вы получаете один выстрел, - говорит Джеффри Вэй, который развивал терапевтические белки в Институте Висса Гарвардского университета.
– Это “обратное методу проб и ошибок, - объясняет он. – Все происходит потому, что мы это программируем.
– Если требуются препараты более точного действия, да ещё с двумя-тремя дополнительными функциями, то они могут быть получены, – говорит Джеффри.
Но это несовместимо с высокой пропускной способностью, которая используется в промышленности.
– Нужен принципиально иной подход, который требует, - говорит он, – чтобы ученый запроектировал новые функции модели и вычислил, как они взаимодействуют.
Способ построения лекарственного средства с двумя или тремя различными компонентами имел некоторый успех с эритропоэтином — гормоном, который стимулирует костный мозг, чтобы произвести больше клеток крови. Рецепторы эритропоэтина также существует в других клетках, которые могут вызвать нежелательные эффекты, если эритропоэтин свяжется с ними. Таким образом, был достигнут эффект в сочетании с видоизмененным геном эритропоэтина с геном – фрагментом антитела. Мутировавший гормон имеет меньшую близость к своему рецептору, который кажется нелогичным. Однако
– Антитела, определяют, какой препарат связывает и пристреливает протеин непосредственно эритроцитов и прекурсоров, что заметно ограничивает побочные эффекты, – объясняет[6]. Этот подход был впоследствии применен к интерферону-альфа и другим цитокинам. Этот метод проверяется с использованием суперкомпьютера, который обрабатывает модель с тысячами итераций и вычисляет, как поведет себя новое лекарство в организме человека.
Лаборатория Вэя, в который он работает вместе со своей женой, Пэм Силвер, недавно была увенчана грантом от Агентства Передовых Оборонных Исследовательских Проектов (DARPA), которое базируется в Арлингтоне, штат Вирджиния. Перед лабораторией была поставлена задача разработки бактерий, которые можно принимать как таблетки, чтобы обеспечить защиту от диареи путешественников – то, что неизменно поражает солдат, когда они развернуты за рубежом. Цель состоит в том, чтобы спроектировать бактерии лечащие воспаление желудочно-кишечного тракта, вызванного патогенными бактериями, убивая возбудителей и выпускать противовоспалительные препараты. Команда выиграла грант, показав, что они смогли переключиться на ген в одной из кишечных бактерий мышей путем введения препарата[7]
Финансирование от DARPA направлено на передовые области науки и технологии, которые применяется для военных. Предыдущие успехи агентства включают развитие интернета и глобальной системы позиционирования (GPS технологии). Но DARPA все чаще обращает свое внимание к биологии, и недавно создал отдел биологических технологий. Как можно выразиться: «Биология-это технология будущего – углерод-кремний нового века».
DARPA помогает ученым достичь новых горизонтов. Это даст команде Висс до 4,7 млн. долларов США для их работы над проектом «диарея путешественников», например.
– Что мне нравится в DARPA? То, что они вынуждают вас быть разными, и они дают вам много денег, - говорит Джеффри. В то же время они установили очень высокую планку и ожидают, что люди потерпят неудачу.
– Если исследования, которые они финансируют не банкротятся какое-то время, то DARPA представляют, что они не сильно рискуют, - говорит он.
Для проекта «диарея путешественников», в DARPA уже постановили, что должно быть пять различных видов бактерий, которые работают вместе, чтобы имело смысл лечить воспаление кишечника.
– В этой системе, когда пять видов вместе они могут расти, но когда они далеко друг от друга они умрут. Ведь первоначально был разработан только один вид, который может эволюционировать, – объясняет Джеффри.
Поэтому команда Висс должны создать сообщество из пяти со-зависимых видов бактерий, которые также ведут себя, как диагностику и лекарства — не просто подвиг.
– Это было решение ДАРПА и это бесспорно, - говорит Джеффри Вэй.
Но DARPA имеет веские основания для требования такой сложности. Есть этические соображения, когда синтетическая биология используется именно так. Забота здесь состоит в том, что создали мутантные породы, которые могут посеять хаос в дикой природе.
– ДАРПА хочет создания организмов, которые являются безопасными для выпуска в окружающую среду — они должны умереть, когда они вдруг окажутся в неположенном месте, и они не должны обмениваться ДНК с другими организмами, – говорит Вэй. С такой умной задачей, он считает, следует считаться, ведь это может помешать им вырваться на волю, хотя он считает, что угрозу для окружающей среды является гипотетической.
Вдаль от этого мира
Сохранение здоровья с помощью микрофлоры необходимо не только солдатам – это тоже важно для космонавтов.
– Понимание микрофлоры является невероятно важным для здоровья человека, поэтому возможность управлять ею в течение длительного космического полета – наиважнейшая задача, - говорит Джон Хоган, ученый-эколог в научно-исследовательском центре Эймса НАСА в Моффетт Филд, Калифорния.
На данный момент НАСА не проводит исследования, подобно тем, что идут в институтах, таких как Висс. Но у него есть свои собственные чаяния в синтетической биологии.
– Марс является целевым объектом для космических путешествий в течение длительного времени, но мы думаем, что это будет трехлетнее кругосветное путешествие, и важной задачей является задача сохранения здоровья у людей всё это время, – объясняет Хоган.
Исследовательский центр Эймс недавно инвестировал в программу производства «нутрицевтики для Космонавтов», например, чтобы защитить их от высоких уровней радиации в космосе.
– Одна из самых больших проблем для полета на Марс – это количество различных необходимых питательных веществ, - говорит Хоган.
– Как удовлетворить требования астронавта в течение трех лет? Если мы не можем обезопасить их от всего, то мы должны решить некоторые важные задачи.
Исследователи в НАСА работают на основе дрожжевых систем. Дрожжи будут перевозиться как споры, которые могут храниться в течение длительного времени и созранять устойчивость к изменениям окружающей среды. Хоган предложил хранить споры в что-то вроде кетчуп в пакете на вынос.
– Достаточно лишь увлажнить их при необходимости, – говорит он.
– Синтетическая биология призывает NASA, потому что она предлагает уникальный уровень контроля биологических системах, и эти системы являются неимоверно эффективными и способны делать вещи, которые физические или химические системы просто не могут, – говорит Хоган. – Каждый микроорганизм – это тонко настроенная платформы химического синтеза, и она воспроизводит себя снова и снова довольно надежно. Если мы пытаемся создать такую систему с нуля, мы создадим жизнь!
Но Хоган говорит, что в некоторых случаях биологическая система не может быть лучшим вариантом.
– НАСА имеет сильную заинтересованность в производстве лекарств по требованию. Это может быть химические платформы, что просто зависит от того, какая больше подходит, – говорит он. – По этой причине НАСА внимательно следит за проектом ДАРПА для военной медицины. Целью проекта является разработка миниатюрных платформ, устройств и методов, в которые может произвести множественные мелкие молекулы активных фармацевтических ингредиентов и терапевтических белков в ответ на конкретные угрозы боя и медицинских потребностей по мере их возникновения.
Гранты для проекта пошли по пути развития как химических, так и биологических систем. Одним из центров, который получил финансирование в Массачусетском технологическом институте (МТИ), который работает на биологические системы. Крис Лав, инженер-химик, который руководит проектом в массачусетском технологическом институте, говорит, что он затрагивает более широкий вопрос:
– Как получить лекарства для пациентов, там и тогда где и гогда они понадобятся. Например, во время стихийных бедствий, таких как ураган "Катрина", который обрушился на штат Луизиана в 2005 году, когда тысячи пациентом потребовался инсулин, но там были технические проблемы его доставки, такие как отсутствие холодильных установок, а много инсулина пропало, – говорит Лав. Так его команда пытается сделать переносные системы, в которых можно производить биологические препараты по требованию в течение 24-48 часов.
– Мы сделали пару молекул и показали целесообразность, - говорит Лав, исследования которого более двух лет финансирует ДАРПА.
В настоящее время многие терапевтические белки, такие как моноклональные антитела продуцируются в клеточной системе млекопитающих, но команда Лава, как и многие другие, выбрала дрожжи, как основную систему.
– Репликации микробных систем очень быстры, а достижения синтетической биологи позволяют нам программировать дрожжи для получения более гуманизированных белков, - говорит он.
Одно из требований заключается в том, что система должна быть небольшой и легко транспортироваться.
– Изначально цель состояла в том, чтобы поместить его в рюкзак, но сейчас, вероятнее, это будет размещено лишь в багажнике машины или джипа, –говорит Лав.
Он возлагает большие надежды на то, компактность гибкой производственной единицы, которая может означать много для медицины и научных исследований. Такие мини установки были бы значительно дешевле, чем крупные производственные подразделения, которые стоят сотни миллионов долларов. И это означает, что малые количества лекарственных средств, которые могут быть необходимы для лечения редких заболеваний, было бы гораздо легче вырабатывать и принимать на месте лечения пациентов.
Лав также считает, что система может быть применима на ранней стадии клинических испытаний. Представьте, что врач, работающий в больнице, думает, что у него обнаружили новые терапевтические антитела и имеет многообещающие данные из исследования мыши. Вместо того, чтобы взять находя в фармацевтической компании, врач может выявить соответствующие гены и отправки последовательности ДНК к биотехнологической компании, которые могут отправить обратно заказ производство системы, которая производит антитела по требованию. И система может быть расположена на территории больницы.
– Разве это не удивительно? – Вопрошает Лав.
В конечном счете, однако, истинная сила синтетической биологии может быть представлена не только в медицине.
– Конечно, синтетическая биология дает большой толчок для разработки медицинских препаратов, но я почти вижу, низко висящие плоды, - говорит Ньюман из Амириса.
Его компания успешно производит синтетическое, возобновляемое биотопливо.
– Биотопливо на сегодня дороже, чем бензин, поэтому перевести машины на выращенное на плантациях топливо не выйдет. Вот где раздолье методам новой науки. Однако через 100-150 лет когда в мире закончится нефть, мы должны подготовить синтетический метод производства бензина, в противном случае будет невиданная война и голод, – говорит Ньюман. – Синтетическая биология будет иметь большой шанс спасти человечество.
Ссылки
[1]Fleischmann RD, Adams MD, White O et al. Whole-genome random sequencing and assembly of Haemophilus influenzae Rd. Science 1995;269:496–512. doi:10.1126/science.7542800
[2]Venter JC, Adams MD, Myers EW et al. The sequence of the human genome. Science 2001;291:1304–1351. doi:10.1126/science.1058040
[3]Gibson DG, Glass JI, Lartigue, C. et al. Creation of a bacterial cell controlled by a chemically synthesized genome. Science 2010;329:52–56. doi:10.1126/science.1190719
[4]Paddon CJ, Westfall PJ, Pitera DJ et al. High-level semi-synthetic production of the potent antimalarial artemisinin. Nature 2013;496:528–532. doi:10.1038/nature12051
[5]Galanie S, Thodey K, Trenchard IJ et al. Complete biosynthesis of opioids in yeast. Science 2015;349:1095–1100. doi:10.1126/science.aac9373
[6]Taylor ND, Way J, Silver PA et al. Anti-glycophorin single-chain Fv fusion to low-affinity mutant erythropoietin improves red blood cell-lineage specificity. Protein Engineering, Design and Selection 2015;23:251–260. doi:10.1093/protein/gzp085
[7]Kotula JW, Kerns SJ, Shaket LA et al. Programmable bacteria detect and record an environmental signal in the mammalian gut. Proceedings of the National Academy of Sciences USA 2014;111:4838–4843. doi:10.1073/pnas.1321321111